Ninlaro (Iksazomib)
Indikasjoner 1 1. Ninlaro preparatomtale (03.11.23). Tilgjengelig på www.legemiddelsok.no
Ninlaro (Iksazomib) er godkjent for bruk i kombinasjon med lenalidomid og deksametasjon til behandling av voksne med myelomatose som har mottatt minst én tidligere behandling.
Dosering 1 1. Ninlaro preparatomtale (03.11.23). Tilgjengelig på www.legemiddelsok.no
Behandling må startes opp og overvåkes av en lege med erfaring i håndtering av myelomatose.
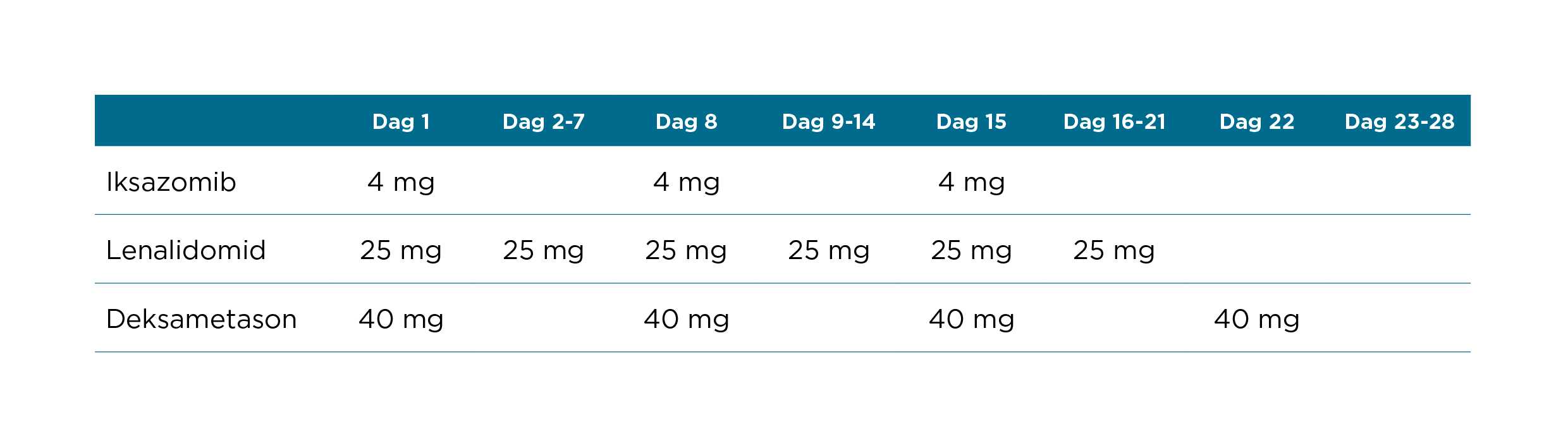
Anbefalt startdose av iksazomib er 4mg en gang i uken på dag 1, 8 og 15 i en 28-dagers behandlingssyklus. Anbefalt startdose for lenalidomid er 25mg daglig på dag 1-21 i en 28-dagers behandlingssyklus. Anbefalt startdose for deksametason er 40mg på dag 1, 8, 15 og 22 i en 28-dagers behandlingssyklus.

Før oppstart av en ny behandlingssyklus:
- Absolutt antall nøytrofile bør være ³ 1000/mm3
- Antall blodplater bør være ³ 75 000/mm3
- Ikke-hematologisk toksisitet bør, basert på legens vurdering, generelt være gjenopprettet til pasientens baseline eller ≤ grad 1
Behandling bør fortsettes inntil sykdomsprogresjon eller uakseptabel toksisitet. Behandling med iksazomib i kombinasjon med lenalidomid og deksametason i mer enn 24 sykluser skal baseres på en individuell nytte-risikovurdering, siden data for toleranse og toksisitet utover 24 sykluser er begrenset.
Doseendringer 1 1. Ninlaro preparatomtale (03.11.23). Tilgjengelig på www.legemiddelsok.no
Se preparatomtale for utfyllende infromasjon om doseendringer for spesielle pasientpopulasjoner, hematologisk toksisitet, utslett og nevropati.
Bivirkninger 1 1. Ninlaro preparatomtale (03.11.23). Tilgjengelig på www.legemiddelsok.no
De hyppigst rapporterte bivirkningene (³ 20%) hos 418 pasienter behandlet i iksazomib-regimet og 417 pasienter behandlet i placebo-regimet var diaré (47% vs 38%) trombocytopeni (41% vs 24%), nøytropeni (37% vs 36%), forstoppelse (31% vs 24%), infeksjon i øvre luftveier (28% vs 24%), perifer nevropati (28% vs 22%), kvalme (28% vs 20%), ryggsmerter (25% vs 21%), utslett (25% vs 15%), perifert ødem (24% vs 19%), oppkast (23% vs 12%) og bronkitt (20% vs 15%). Alvorlige bivirkninger rapportert hos ³ 2% av pasienter inkluderte diaré (3%), trombocytopeni (2%) og bronkitt (2%).
Pakninger og priser 2 2. NINLARO felleskatalogtekst. Tilgjengelig på: https://www.felleskatalogen.no/medisin/ninlaro-takeda-633676
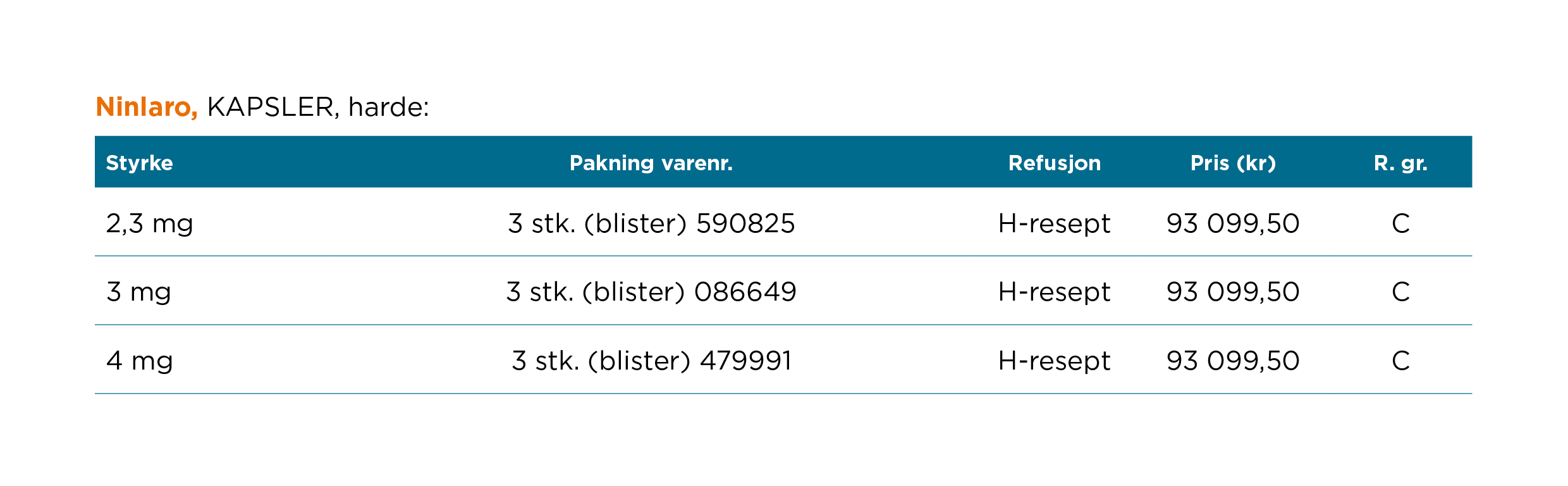
Refusjon: H-resept rekvirering skal gjøres i tråd med nasjonale handlingsprogrammer for kreft of føringer fra RHF/LIS spesialistgruppe. Vilkår: (216) Refusjon ytes kun etter resept fra sykehuslege eller avtalespesialist. Reseptgruppe: C
Godkjent for bruk av beslutningsforum 2 2. NINLARO felleskatalogtekst. Tilgjengelig på: https://www.felleskatalogen.no/medisin/ninlaro-takeda-633676 : - Ninlaro i kombinasjon med deksametasjon og lenalidomid kan innføres til behandling av refraktær eller residiv myelomatose etter minst tre tidligere behandlinger.
For fullstendig oversikt over kontraindikasjoner, forsiktighetsregler, interaksjoner og bivirkninger, se preparatomtale.
Sist oppdatert 02.06.25



